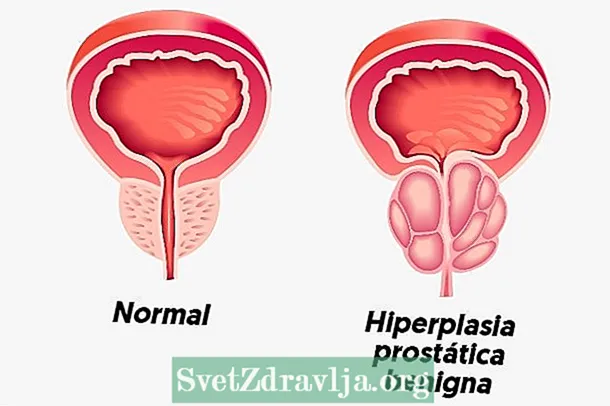
Sulfate de chondroïtine
Auteur:
Alice Brown
Date De Création:
1 Peut 2021
Date De Mise À Jour:
9 Juillet 2025

Contenu
- Peut-être efficace pour...
- Preuves insuffisantes pour évaluer l'efficacité de...
- Précautions particulières et mises en garde :
Certains produits à base de sulfate de chondroïtine ne sont pas étiquetés avec précision. Dans certains cas, la quantité de chondroïtine a varié de zéro à plus de 100 % de la quantité indiquée sur l'étiquette du produit. De plus, certains produits contiennent de la chondroïtine provenant de plusieurs animaux différents, même si cela n'est pas toujours indiqué sur l'étiquette.
Le sulfate de chondroïtine est utilisé pour l'arthrose et la cataracte. Il est souvent utilisé en combinaison avec d'autres ingrédients, notamment l'ascorbate de manganèse, l'acide hyaluronique, les peptides de collagène ou la glucosamine. Le sulfate de chondroïtine est également pris par voie orale, appliqué sur la peau et administré en injection pour de nombreuses autres affections, mais il n'existe aucune preuve scientifique solide à l'appui de ces utilisations.
Base de données complète de médecines naturelles évalue l'efficacité sur la base de preuves scientifiques selon l'échelle suivante : Efficace, Probablement efficace, Peut-être efficace, Peut-être inefficace, Probablement inefficace, Inefficace et Preuves insuffisantes pour évaluer.
Les cotes d'efficacité pour SULFATE DE CHONDROÏTINE sont les suivants:
Peut-être efficace pour...
- Cataractes. La recherche montre que l'injection d'une solution contenant du sulfate de chondroïtine et de l'hyaluronate de sodium dans l'œil protège l'œil pendant la chirurgie de la cataracte. De nombreux produits différents contenant du sulfate de chondroïtine et de l'hyaluronate de sodium ont été examinés par la Food and Drug Administration (FDA) des États-Unis pour une utilisation pendant la chirurgie de la cataracte. Cependant, il n'est pas clair si l'ajout de sulfate de chondroïtine aux solutions d'hyaluronate de sodium aide à réduire la pression dans l'œil après une chirurgie de la cataracte par rapport à d'autres traitements similaires. Certaines premières études suggèrent qu'une solution oculaire spécifique contenant du sulfate de chondroïtine et de l'hyaluronate (Viscoat, Laboratoires Alcon) peut diminuer la pression dans l'œil et améliorer la santé globale des yeux après l'ablation de la cataracte. Cependant, les gouttes ne semblent pas être meilleures que les gouttes contenant du hyaluronate seul ou un autre produit chimique appelé hydroxypropylméthyl-cellulose. L'effet des solutions contenant uniquement du sulfate de chondroïtine sur la chirurgie de la cataracte n'est pas connu.
- Arthrose. La recherche clinique montre que la prise de sulfate de chondroïtine par voie orale améliore légèrement la douleur et la fonction chez certaines personnes souffrant d'arthrose lorsqu'elle est utilisée jusqu'à 6 mois. Il semble fonctionner mieux chez les personnes souffrant de douleurs plus intenses et lorsqu'une préparation de qualité pharmaceutique est utilisée. Les produits spécifiques qui se sont avérés bénéfiques chez les patients souffrant d'arthrose comprennent Chondrosulf (IBSA Institut Biochimique SA), Chondrosan (Bioibérica, S.A.) et Structrum (Laboratoires Pierre Fabre). Mais le soulagement de la douleur est susceptible d'être au mieux faible. D'autres recherches montrent que la prise de sulfate de chondroïtine jusqu'à 2 ans pourrait ralentir la progression de l'arthrose.
Certaines recherches ont évalué les effets du sulfate de chondroïtine lorsqu'il est pris par voie orale en combinaison avec de la glucosamine. Certaines recherches montrent que la prise de produits spécifiques contenant du sulfate de chondroïtine et de la glucosamine aide à réduire les symptômes de l'arthrose. D'autres recherches ne montrent aucun avantage lorsque des préparations non commerciales sont utilisées. La prise à long terme de sulfate de chondroïtine et de glucosamine semble ralentir la progression de l'arthrose.
Il existe des preuves qu'une crème pour la peau contenant du sulfate de chondroïtine en combinaison avec du sulfate de glucosamine, du cartilage de requin et du camphre peut réduire les symptômes de l'arthrose. Cependant, tout soulagement des symptômes est probablement dû au camphre et non aux autres ingrédients. Il n'y a aucune recherche montrant que la chondroïtine est absorbée par la peau.
Preuves insuffisantes pour évaluer l'efficacité de...
- Douleurs articulaires causées par des médicaments appelés inhibiteurs de l'aromatase (arthralgies induites par les inhibiteurs de l'aromatase). Les premières recherches suggèrent que la prise d'une combinaison de sulfate de glucosamine et de sulfate de chondroïtine en deux ou trois doses fractionnées par jour pendant 24 semaines améliore les douleurs articulaires et les symptômes causés par les médicaments utilisés pour traiter le cancer du sein.
- œil sec. Les premières recherches montrent que l'utilisation de gouttes oculaires au sulfate de chondroïtine peut réduire la sécheresse oculaire. D'autres recherches montrent que l'utilisation de gouttes oculaires contenant du sulfate de chondroïtine et de la gomme de xanthane peut améliorer la sécheresse oculaire ainsi que l'utilisation de larmes artificielles. Mais d'autres premières recherches ne montrent aucun avantage.
- Douleurs musculaires causées par l'exercice. Les premières recherches montrent que la prise quotidienne de sulfate de chondroïtine ne réduit pas les douleurs musculaires après l'exercice chez les hommes.
- Gonflement (inflammation) de l'estomac (gastrite). Les premières recherches montrent que boire un liquide spécifique contenant du sulfate de chondroïtine et de l'acide hyaluronique peut diminuer les douleurs abdominales chez les personnes souffrant de gastrite.
- Syndrome de la vessie douloureuse (cystite interstitielle). Certaines recherches montrent que mettre du liquide contenant du sulfate de chondroïtine dans la vessie peut améliorer les symptômes douloureux de la vessie. Mais la plupart de ces études sont de faible qualité. Certaines études de meilleure qualité suggèrent que l'utilisation de sulfate de chondroïtine à l'intérieur de la vessie n'est pas bénéfique. Certaines premières recherches montrent que la prise d'un produit contenant du sulfate de chondroïtine et d'autres ingrédients par voie orale peut améliorer la vessie douloureuse. Mais il n'est pas clair si le bénéfice provient du sulfate de chondroïtine ou des autres ingrédients.
- Un trouble qui affecte les os et les articulations, généralement chez les personnes présentant une carence en sélénium (maladie de Kashin-Beck). Les premières recherches suggèrent que le sulfate de chondroïtine, avec ou sans chlorhydrate de glucosamine, peut réduire la douleur chez les personnes atteintes de la maladie de Kashin-Beck. En outre, la prise de sulfate de chondroïtine avec du sulfate de glucosamine peut ralentir le rétrécissement de l'espace articulaire chez les personnes atteintes de cette maladie osseuse. Cependant, il n'est pas clair si la prise de sulfate de chondroïtine seul ralentit le rétrécissement de l'espace articulaire.
- Attaque cardiaque. Certaines premières recherches montrent que la prise de sulfate de chondroïtine par voie orale pourrait réduire le risque d'avoir une première crise cardiaque ou une crise cardiaque récurrente.
- Peau squameuse et qui démange (psoriasis). Les premières recherches suggèrent que la prise de sulfate de chondroïtine pendant 2-3 mois diminue la douleur et améliore l'état de la peau chez les personnes atteintes de psoriasis. Mais d'autres recherches suggèrent que la prise quotidienne de sulfate de chondroïtine (Condrosan, CS Bio-Active, Bioiberica S.A., Barcelone, Espagne) pendant 3 mois ne réduit pas la gravité du psoriasis chez les personnes atteintes de psoriasis et d'arthrose du genou.
- Perte de contrôle de la vessie (incontinence urinaire). Les premières recherches suggèrent que l'insertion de sulfate de chondroïtine sodique dans la vessie via une sonde urinaire améliore la qualité de vie des personnes souffrant d'hyperactivité vésicale.
- Infections des reins, de la vessie ou de l'urètre (infections des voies urinaires ou infections urinaires). Les premières recherches montrent que l'administration d'une solution contenant du sulfate de chondroïtine et de l'acide hyaluronique dans la vessie via un cathéter réduit le nombre d'infections urinaires chez les femmes ayant des antécédents d'infections urinaires.
- Vieillissement de la peau.
- Brûlures d'estomac persistantes.
- Cardiopathie.
- Taux de cholestérol élevé.
- Os faibles et cassants (ostéoporose).
- Peau ridée.
- D'autres conditions.
Dans l'arthrose, le cartilage des articulations se détériore. La prise de sulfate de chondroïtine, l'un des éléments constitutifs du cartilage, pourrait ralentir cette dégradation.
Lorsqu'il est pris par voie orale: Le sulfate de chondroïtine est PROBABLEMENT SR. Le sulfate de chondroïtine a été pris par voie orale en toute sécurité jusqu'à 6 ans. Cela peut causer de légères douleurs à l'estomac et des nausées. D'autres effets secondaires qui ont été signalés sont des ballonnements, de la diarrhée, de la constipation, des maux de tête, des paupières enflées, un gonflement des jambes, une perte de cheveux, des éruptions cutanées et des battements cardiaques irréguliers.
Lorsqu'il est placé dans l'œil: Le sulfate de chondroïtine est PROBABLEMENT SR lorsqu'il est utilisé comme solution oculaire lors d'une opération de la cataracte.
Lorsqu'il est donné comme un coup: Le sulfate de chondroïtine est ÉVENTUELLEMENT SR lorsqu'il est injecté dans le muscle par injection, à court terme.
Il existe une certaine inquiétude quant à la sécurité du sulfate de chondroïtine, car il provient de sources animales. Certaines personnes craignent que des pratiques de fabrication dangereuses ne conduisent à la contamination des produits à base de chondroïtine par des tissus animaux malades, y compris ceux qui pourraient transmettre l'encéphalopathie spongiforme bovine (maladie de la vache folle). Jusqu'à présent, il n'y a aucun rapport sur la chondroïtine causant une maladie chez l'homme, et le risque est considéré comme faible.
Certains produits à base de chondroïtine contiennent des quantités excessives de manganèse. Renseignez-vous auprès de votre professionnel de la santé sur les marques fiables.
Précautions particulières et mises en garde :
La grossesse et l'allaitement: Il n'y a pas assez d'informations fiables pour savoir si le sulfate de chondroïtine est sûr à utiliser pendant la grossesse ou l'allaitement. Restez prudent et évitez de l'utiliser.Asthme: Certains craignent que le sulfate de chondroïtine n'aggrave l'asthme. Si vous souffrez d'asthme, utilisez le sulfate de chondroïtine avec prudence.
Troubles de la coagulation sanguine: En théorie, l'administration de sulfate de chondroïtine pourrait augmenter le risque de saignement chez les personnes atteintes de troubles de la coagulation sanguine.
Cancer de la prostate: Les premières recherches suggèrent que la chondroïtine pourrait provoquer la propagation ou la récurrence du cancer de la prostate. Cet effet n'a pas été démontré avec les suppléments de sulfate de chondroïtine. Cependant, jusqu'à ce que l'on en sache plus, ne prenez pas de sulfate de chondroïtine si vous avez un cancer de la prostate ou si vous présentez un risque élevé de le développer (vous avez un frère ou un père atteint d'un cancer de la prostate).
- Modérer
- Soyez prudent avec cette combinaison.
- Warfarine (Coumadin)
- La warfarine (Coumadin) est utilisée pour ralentir la coagulation du sang. Il existe plusieurs rapports montrant que la prise de chondroïtine avec de la glucosamine augmente l'effet de la warfarine (Coumadin) sur la coagulation du sang. Cela peut provoquer des ecchymoses et des saignements qui peuvent être graves. Ne prenez pas de chondroïtine si vous prenez de la warfarine (Coumadin).
- Il n'y a pas d'interactions connues avec les herbes et les suppléments.
- Il n'y a pas d'interactions connues avec les aliments.
PAR LA BOUCHE:
- Pour l'arthrose: La dose typique de sulfate de chondroïtine est de 800 à 2000 mg pris en une seule dose ou en deux ou trois doses fractionnées par jour pendant jusqu'à 3 ans.
- Pour l'arthrose: Une crème contenant 50 mg/gramme de sulfate de chondroïtine, 30 mg/gramme de sulfate de glucosamine, 140 mg/gramme de cartilage de requin et 32 mg/gramme de camphre a été utilisée au besoin pour les articulations douloureuses jusqu'à 8 semaines.
- Pour l'arthrose: Du sulfate de chondroïtine (Matrix) a été injecté dans le muscle quotidiennement ou deux fois par semaine pendant 6 mois.
- Pour les cataractes: Plusieurs collyres différents contenant de l'hyaluronate de sodium et du sulfate de chondroïtine (DisCoVisc, Laboratoires Alcon ; Viscoat, Laboratoires Alcon ; DuoVisc, Laboratoires Alcon ; Viscoat, Laboratoires Alcon ; Provisc, Laboratoires Alcon) ont été utilisés pendant la chirurgie de la cataracte.
Pour en savoir plus sur la façon dont cet article a été rédigé, veuillez consulter le Base de données complète de médecines naturelles méthodologie.
- Bruyère O, Honvo G, Véronèse N, et al. Une recommandation d'algorithme mise à jour pour la gestion de l'arthrose du genou de la Société européenne pour les aspects cliniques et économiques de l'ostéoporose, de l'arthrose et des maladies musculo-squelettiques (ESCEO). Semin Arthrite Rheum. Déc 2019 : 49 : 337-50. Voir résumé.
- Navarro SL, Levy L, Curtis KR, Lampe JW, Hullar MAJ. Modulation du microbiote intestinal par la glucosamine et la chondroïtine dans un essai pilote randomisé en double aveugle chez l'homme. Micro-organismes. 2019 novembre 23;7. pii: E610. Voir résumé.
- Restaino OF, Finamore R, Stellavato A, et al. Compléments alimentaires européens de sulfate de chondroïtine et de glucosamine : Une évaluation systématique de la qualité et de la quantité par rapport aux produits pharmaceutiques. Glucides Polym. 15 octobre 2019 ; 222:114984. Voir résumé.
- Kolasinski SL, Neogi T, Hochberg MC, et al. Lignes directrices 2019 de l'American College of Rheumatology/Arthritis Foundation pour la prise en charge de l'arthrose de la main, de la hanche et du genou. Arthrite Rheumatol. 2020 février ; 72 : 220-33. Voir résumé.
- Savarino V, Pace F2, Scarpignato C; Groupe d'étude Esoxx. Essai clinique randomisé : protection des muqueuses associée à la suppression de l'acidité dans le traitement du reflux non érosif - efficacité d'Esoxx, une formulation bioadhésive à base d'acide hyaluronique et de sulfate de chondroïtine. Aliment Pharmacol Ther. 2017;45:631-642. Voir résumé.
- Goddard JC, Janssen DAW. Acide hyaluronique intravésical et sulfate de chondroïtine pour les infections récurrentes des voies urinaires : revue systématique et méta-analyse. Int Urogynecol J. 2018 Juil;29:933-942. Epub 2017 nov. 27. Critique. Voir résumé.
- Iannitti T, Morales-Medina JC, Merighi A, et al. Un dispositif médical à base d'acide hyaluronique et de sulfate de chondroïtine améliore la douleur, l'inconfort et les caractéristiques endoscopiques de la gastrite. Drug Deliv Transl Res. 8 octobre 2018 : 994-999. Voir résumé.
- Tsuruta A, Horiike T, Yoshimura M, Nagaoka I. Évaluation de l'effet de l'administration d'un supplément contenant de la glucosamine sur les biomarqueurs du métabolisme du cartilage chez les joueurs de football : étude randomisée en double aveugle contre placebo. Mol Med Rep. 2018 Oct;18:3941-3948. Publication en ligne du 17 août 2018. Voir le résumé.
- Simental-Mendía M, Sánchez-García A, Vilchez-Cavazos F, Acosta-Olivo CA, Peña-Martínez VM, Simental-Mendía LE. Effet de la glucosamine et du sulfate de chondroïtine dans l'arthrose symptomatique du genou: une revue systématique et une méta-analyse d'essais randomisés contrôlés par placebo. Rheumatol Int. Août 2018 ; 38 : 1413-1428. Publication en ligne du 11 juin 2018. Critique. Voir résumé.
- Ogata T, Ideno Y, Akai M, et al. Effets de la glucosamine chez les patients souffrant d'arthrose du genou: une revue systématique et une méta-analyse. Clin Rheumatol. Septembre 2018 ; 37 : 2479-2487. Publication en ligne du 30 avril 2018. Voir le résumé.
- Pyo JS, Cho WJ. Revue systématique et méta-analyse de l'acide hyaluronique intravésical et de l'instillation d'acide hyaluronique/sulfate de chondroïtine pour la cystite interstitielle/syndrome de la vessie douloureuse. Cell Physiol Biochem. 2016;39:1618-25. Voir résumé.
- Lopez HL, Ziegenfuss TN, Park J. Évaluation des effets du collagène BioCell, un nouvel extrait de cartilage, sur le soutien du tissu conjonctif et la récupération fonctionnelle après l'exercice. Intégrer Med (Encinitas). 2015;14:30-8. Voir résumé.
- Pérez-Balbuena AL, Ochoa-Tabares JC, Belalcazar-Rey S, et al. Efficacité d'une association fixe de 0,09 % de gomme xanthane/0,1 % de sulfate de chondroïtine sans conservateur vs polyéthylène glycol/propylène glycol chez des sujets atteints de sécheresse oculaire : un essai contrôlé randomisé multicentrique. BMC Ophtalmol. 2016 septembre;16:164.Voir résumé.
- Zeng C, Wei J, Li H, et al. Efficacité et innocuité de la Glucosamine, de la chondroïtine, les deux en association, ou du célécoxib dans le traitement de l'arthrose du genou. Sci Rep. 2015;5:16827. Voir résumé.
- Roman-Blas JA, Castañeda S, Sánchez-Pernaute O, et al. Le traitement combiné avec du sulfate de chondroïtine et du sulfate de glucosamine ne montre aucune supériorité par rapport au placebo pour la réduction des douleurs articulaires et des troubles fonctionnels chez les patients atteints d'arthrose du genou : un essai clinique multicentrique, randomisé, à double insu et contrôlé par placebo pendant six mois. Arthrite Rheumatol. 2017;69:77-85. Voir résumé.
- Pelletier JP, Raynauld JP, Beaulieu AD, et al. Efficacité du sulfate de chondroïtine par rapport au célécoxib sur les modifications structurelles de l'arthrose du genou à l'aide de l'imagerie par résonance magnétique : une étude exploratoire multicentrique de 2 ans. Arthrite Res Ther. 2016;18:256. Voir résumé.
- Singh JA, Noorbaloochi S, MacDonald R, Maxwell LJ. Chondroïtine pour l'arthrose. Cochrane Database Syst Rév. 2015 28 janvier;1:CD005614. Voir résumé.
- Bruyère O, Cooper C, Pelletier JP, et al. Une déclaration de consensus sur l'algorithme de la Société européenne pour les aspects cliniques et économiques de l'ostéoporose et de l'arthrose (ESCEO) pour la gestion de l'arthrose du genou - De la médecine factuelle à la réalité. Semin Arthrite Rheum. 2016;45(4 Suppl):S3-11. Voir résumé.
- Reginster JY, Dudler J, Blicharski T, Pavelka K. Le sulfate de chondroïtine de qualité pharmaceutique est aussi efficace que le célécoxib et supérieur au placebo dans l'arthrose symptomatique du genou : l'essai ChONdroitin versus CElecoxib versus Placebo (CONCEPT). Ann Rheum Dis. 22 mai 2017. pii : annrheumdis-2016-210860. Voir résumé.
- Volpi N. Qualité des différentes préparations de sulfate de chondroïtine par rapport à leur activité thérapeutique. J Pharm Pharmacol 2009;61:1271-80. Voir résumé.
- Lauder RM. Sulfate de chondroïtine : une molécule complexe avec des impacts potentiels sur un large éventail de systèmes biologiques. Complément Ther Med 2009;17:56-62. Voir résumé.
- Barnhill JG, Fye CL, Williams DW, Reda DJ, Harris CL, Clegg DO. Sélection de produits de chondroïtine pour l'essai d'intervention sur l'arthrite glucosamine/chondroïtine. J Am Pharm Assoc 2006;46:14-24. Voir résumé.
- Zegels B, Crozes P, Uebelhart D, Bruyère O, Reginster JY. Équivalence d'une dose unique (1200 mg) par rapport à une dose trois fois par jour (400 mg) de sulfate de chondroïtine 4&6 chez les patients atteints d'arthrose du genou. Résultats d'une étude randomisée en double aveugle contre placebo. Arthrose Cartilage 2013;21:22-7. Voir résumé.
- Vigan M. Dermite de contact allergique causée par le sulfate de chondroïtine sodique contenu dans une crème cosmétique. Dermatite de contact 2014;70:383-4. Voir résumé.
- Torella M, Schettino MT, Salvatore S, Serati M, De Franciscis P, Colacurci N. Thérapie intravésicale dans la cystite récurrente: une expérience multicentrique. J Infect Chemother 2013;19:920-5. Voir résumé.
- Schneider H, Maheu E, Cucherat M. Effet modificateur des symptômes du sulfate de chondroïtine dans l'arthrose du genou: une méta-analyse d'essais randomisés contrôlés par placebo réalisés avec structum(®). Ouvrir Rheumatol J. 2012;6:183-9. Voir résumé.
- Palmieri B, Merighi A, Corbascio D, Rottigni V, Fistetto G, Esposito A. Combinaison fixe d'acide hyaluronique et de formulation orale de sulfate de chondroïtine dans une étude randomisée en double aveugle, contrôlée par placebo pour le traitement des symptômes chez les patients atteints de troubles gastro-œsophagiens non érosifs reflux. Eur Rev Med Pharmacol Sci 2013;17:3272-8. Voir résumé.
- Llamas-Moreno JF, Baiza-Durán LM, Saucedo-Rodríguez LR, Alaníz-De la O JF. Efficacité et sécurité du sulfate de chondroïtine/gomme xanthane versus polyéthylène glycol/propylène glycol/hydroxypropyl guar chez les patients souffrant de sécheresse oculaire. Clin Ophthalmol 2013;7:995-9. Voir résumé.
- De Vita D, Antell H, Giordano S. Efficacité de l'acide hyaluronique intravésical avec ou sans sulfate de chondroïtine pour la cystite bactérienne récurrente chez la femme adulte : une méta-analyse. Int Urogynecol J 2013;24:545-52. Voir résumé.
- Greenlee H, Crew KD, Shao T, Kranwinkel G, Kalinsky K, Maurer M, Brafman L, Insel B, Tsai WY, Hershman DL. Étude de phase II de la glucosamine avec la chondroïtine sur les symptômes articulaires associés aux inhibiteurs de l'aromatase chez les femmes atteintes d'un cancer du sein. Support Care Cancer 2013;21:1077-87. Voir résumé.
- Fransen M, Agaliotis M, Nairn L, Votrubec M, Bridgett L, Su S, Jan S, March L, Edmonds J, Norton R, Woodward M, Day R; Groupe collaboratif d'étude LEGS. Glucosamine et chondroïtine pour l'arthrose du genou : un essai clinique randomisé en double aveugle contre placebo évaluant des régimes simples et combinés. Ann Rheum Dis 2015;74:851-8. Voir résumé.
- Provenza JR, Shinjo SK, Silva JM, Peron CR, Rocha FA. La glucosamine et le sulfate de chondroïtine combinés, une ou trois fois par jour, procurent une analgésie cliniquement pertinente dans l'arthrose du genou. Clin Rheumatol 2015;34:1455-62.Voir le résumé.
- von Felden J, Montani M, Kessebohm K, Stickel F. Lésion hépatique aiguë induite par un médicament imitant une hépatite auto-immune après la prise de compléments alimentaires contenant de la glucosamine et du sulfate de chondroïtine. Int J Clin Pharmacol Ther 2013;51:219-23. Voir résumé.
- Hochberg MC, Martel-Pelletier J, Monfort J, Möller I, Castillo JR, Arden N,Berenbaum F, Blanco FJ, Conaghan PG, Doménech G, Henrotin Y, Pap T, Richette P, Sawitzke A, du Souich P, Pelletier JP ; au nom du groupe d'enquête MOVES. Chondroïtine sulfate et glucosamine associés dans la gonarthrose douloureuse : un essai multicentrique, randomisé, en double aveugle, de non-infériorité versus célécoxib. Ann Rheum Dis 2016;75:37-44. Voir résumé.
- Cerda C, Bruguera M, Parés A. Hépatotoxicité associée à la glucosamine et au sulfate de chondroïtine chez les patients atteints d'une maladie hépatique chronique. Monde J Gastroenterol 2013;19:5381-4. Voir résumé.
- Bray HG, Gregory JE, Stacey M. Chimie des tissus. 1. La chondroïtine du cartilage. Biochem J 1944;38:142-146.
- FDA. Approbation préalable à la commercialisation (PMA). Disponible sur : http://www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfpma/pma.cfm?id=20196.
- La FDA accorde une approbation de pré-commercialisation pour Viscoat. Normes de sécurité Biomed 1986;16:82.
- Blotman F et Loyau G. Essai clinique avec du sulfate de chondroïtine dans la gonarthrose [résumé]. Chariot pour l'arthrose 1993 ; 1 : 68.
- Adebowale AO, Cox DS Liang Z Eddington ND. Analyse de la teneur en glucosamine et en sulfate de chondroïtine des produits commercialisés et de la perméabilité au caco-2 des matières premières en sulfate de chondroïtine. J Am Assoc. nutraceutique. 2000;3:37-44.
- Pavelka et et al. Etude dose-effet en double aveugle des cs 4 & 6 par voie orale 1200mg, 800mg, 200mg contre placebo dans le traitement de l'arthrose fémoro-tibiale. Wular Rheumatol Litre 1998;27(suppl 2):63.
- L'Hirondel JL. [Etude clinique en double aveugle avec application orale de sulfate de chondroïtine versus placebo pour le traitement de la gonarthrose fémorale tibio chez 125 patients]. Litera Rheumatologica 1992;14:77-84.
- Fleisch, AM, Merlin C, Imhoff A et et al. Une étude randomisée, en double aveugle et contrôlée par placebo d'un an avec du sulfate de chondroïtine par voie orale chez des patients atteints d'arthrose du genou. Arthrose et cartilage 1997;5:70.
- Uebelhart D et Chantraine A. Efficacite clinique du sulfate de chondroïtine dans la gonarthrose : Etude randomisée en double-insu versus placebo [résumé]. Rev.Rhumatisme 1994;10:692.
- Verbruggen, G., Goemaere, S. et Veys, E. M. Sulfate de chondroïtine : S/DMOAD (médicament anti-arthrose modifiant la structure/la maladie) dans le traitement de l'arthrose des articulations des doigts. Arthrose Cartilage 1998;6 Suppl A:37-38. Voir résumé.
- Nakazawa, K., Murata, K., Izuka, K. et Oshima, Y. Les effets à court terme des sulfates de chondroïtine A et C sur les sujets athérosclérotiques coronaires : en référence à ses activités anti-thrombogènes. Jpn.Heart J 1969;10:289-296. Voir résumé.
- Nakazawa, K. et Murata, K. Étude comparative des effets des isomères de sulfate de chondroïtine sur des sujets athérosclérotiques. ZFA. 1979;34:153-159. Voir résumé.
- Thilo, G. [Une étude de 35 cas d'arthrose traités avec de l'acide sulfurique chondrotiine (traduction de l'auteur)]. Schweizerische Rundschau fur Medizin Praxis 12-27-1977;66:1696-1699. Voir résumé.
- Embriano, P. J. Pressions postopératoires après phacoémulsification : hyaluronate de sodium vs chondroïtine sulfate de sodium-hyaluronate de sodium. Ann.Ophthalmol. 1989;21:85-88, 90. Voir le résumé.
- Railhac, JJ, Zaim, M., Saurel, AS, Vial, J. et Fournie, B. Effet d'un traitement de 12 mois avec du sulfate de chondroïtine sur le volume du cartilage chez les patients atteints d'arthrose du genou : un pilote randomisé, en double aveugle, contrôlé par placebo étude par IRM. Clin.Rhumatol. 2012 ; 31 : 1347-1357. Voir résumé.
- De, Vita D. et Giordano, S. Efficacité de l'acide hyaluronique intravésical/sulfate de chondroïtine dans la cystite bactérienne récurrente : une étude randomisée. Int.Urogynecol.J. 2012;23:1707-1713. Voir résumé.
- Nickel, JC, Hanno, P., Kumar, K. et Thomas, H. Deuxième évaluation multicentrique, randomisée, en double aveugle, en groupes parallèles de l'efficacité et de l'innocuité du sulfate de chondroïtine sodique intravésical par rapport au témoin inactif du véhicule chez les sujets avec interstitiel syndrome de cystite/douleur vésicale. Urologie 2012;79:1220-1224. Voir résumé.
- Yue, J., Yang, M., Yi, S., Dong, B., Li, W., Yang, Z., Lu, J., Zhang, R. et Yong, J. Chondroïtine sulfate et/ou chlorhydrate de glucosamine pour la maladie de Kashin-Beck : une étude randomisée en grappes et contrôlée par placebo. Arthrose.Cartilage. 2012;20:622-629. Voir résumé.
- Kanzaki, N., Saito, K., Maeda, A., Kitagawa, Y., Kiso, Y., Watanabe, K., Tomonaga, A., Nagaoka, I., et Yamaguchi, H. Effet d'un complément alimentaire contenant du chlorhydrate de glucosamine, du sulfate de chondroïtine et des glycosides de quercétine sur l'arthrose symptomatique du genou : une étude randomisée, en double aveugle, contrôlée par placebo. J.Sci.Food Agric. 15-3-2012;92:862-869. Voir résumé.
- Wildi, LM, Raynauld, JP, Martel-Pelletier, J., Beaulieu, A., Bessette, L., Morin, F., Abram, F., Dorais, M., et Pelletier, JP Le sulfate de chondroïtine réduit à la fois le volume du cartilage perte et lésions de la moelle osseuse chez les patients atteints d'arthrose du genou commençant dès 6 mois après le début du traitement : une étude pilote randomisée, en double aveugle, contrôlée contre placebo utilisant l'IRM. Ann.Rheum.Dis. 2011;70:982-989. Voir résumé.
- Damiano, R., Quarto, G., Bava, I., Ucciero, G., De, Domenico R., Palumbo, MI et Autorino, R. Prévention des infections récurrentes des voies urinaires par administration intravésicale d'acide hyaluronique et de sulfate de chondroïtine : un essai randomisé contrôlé par placebo. Eur.Urol. 2011;59:645-651. Voir résumé.
- Zhou, Q., Chen, H., Qu, M., Wang, Q., Yang, L. et Xie, L. Développement d'un nouveau modèle ex vivo d'adhérence fongique cornéenne. Graefes Arch.Clin.Exp.Ophthalmol. 2011;249:693-700. Voir résumé.
- Liesegang, T. J. Substances viscoélastiques en ophtalmologie. Surv.Ophthalmol. 1990;34:268-293. Voir résumé.
- Furer, V., Wieczorek, R. L. et Pillinger, M. H. Chondrite bilatérale du pavillon de l'oreille précédée de l'initiation d'un supplément de glucosamine chondroïtine. Scand.J.Rheumatol. 2011;40:241-243. Voir résumé.
- Chen, W. C., Yao, C. L., Chu, I. M. et Wei, Y. H. Comparer les effets de la chondrogenèse par culture de cellules souches mésenchymateuses humaines avec divers types de sulfate de chondroïtine C. J.Biosci.Bioeng. 2011;111:226-231. Voir résumé.
- Kato, D., Era, S., Watanabe, I., Arihara, M., Sugiura, N., Kimata, K., Suzuki, Y., Morita, K., Hidari, KI et Suzuki, T. Antiviral activité de la chondroïtine sulfate E ciblant la protéine d'enveloppe du virus de la dengue. Antiviral Res. 2010;88:236-243. Voir résumé.
- Wandel, S., Juni, P., Tendal, B., Nuesch, E., Villiger, PM, Welton, NJ, Reichenbach, S. et Trelle, S. Effets de la glucosamine, de la chondroïtine ou du placebo chez les patients souffrant d'arthrose de la hanche ou du genou : méta-analyse en réseau. BMJ 2010;341:c4675. Voir résumé.
- Rentsch, C., Rentsch, B., Breier, A., Spekl, K., Jung, R., Manthey, S., Scharnweber, D., Zwipp, H. et Biewener, A. défauts de taille traités avec des échafaudages de polycaprolactone-co-lactide issus de l'ingénierie tissulaire : une étude pilote sur des rats. J.Biomed.Mater.Res.A 12-1-2010;95:964-972. Voir résumé.
- Im, A. R., Park, Y. et Kim, Y. S. Isolement et caractérisation des sulfates de chondroïtine de l'esturgeon (Acipenser sinensis) et de leurs effets sur la croissance des fibroblastes. Biol.Pharm.Bull. 2010;33 :1268-1273. Voir résumé.
- Sawitzke, AD, Shi, H., Finco, MF, Dunlop, DD, Harris, CL, Singer, NG, Bradley, JD, Silver, D., Jackson, CG, Lane, NE, Oddis, CV, Wolfe, F. , Lisse, J., Furst, DE, Bingham, CO, Reda, DJ, Moskowitz, RW, Williams, HJ et Clegg, DO Efficacité et sécurité cliniques de la glucosamine, du sulfate de chondroïtine, de leur combinaison, du célécoxib ou du placebo pris pour traiter l'arthrose du genou : résultats à 2 ans de GAIT. Ann.Rheum.Dis. 2010;69:1459-1464. Voir résumé.
- Nickel, JC, Egerdie, RB, Steinhoff, G., Palmer, B. et Hanno, P. Une évaluation pilote multicentrique, randomisée, en double aveugle et en groupes parallèles de l'efficacité et de l'innocuité du sulfate de chondroïtine sodique intravésical par rapport au véhicule témoin dans patients atteints de cystite interstitielle/syndrome de la vessie douloureuse. Urologie 2010;76:804-809. Voir résumé.
- Moller, I., Perez, M., Monfort, J., Benito, P., Cuevas, J., Perna, C., Domenech, G., Herrero, M., Montell, E. et Verges, J. Efficacité du sulfate de chondroïtine chez les patients atteints d'arthrose du genou et de psoriasis concomitants : une étude randomisée, en double aveugle, contrôlée par placebo. Arthrose.Cartilage. 2010;18 Suppl 1:S32-S40. Voir résumé.
- Egea, J., Garcia, A. G., Verges, J., Montell, E. et Lopez, M. G. Actions antioxydantes, anti-inflammatoires et neuroprotectrices du sulfate de chondroïtine et des protéoglycanes. Arthrose.Cartilage. 2010;18 Suppl 1:S24-S27. Voir résumé.
- Hochberg, M. C. Effets modifiant la structure du sulfate de chondroïtine dans l'arthrose du genou : une méta-analyse mise à jour d'essais randomisés contrôlés par placebo d'une durée de 2 ans. Arthrose.Cartilage. 2010;18 Suppl 1:S28-S31. Voir résumé.
- Imada, K., Oka, H., Kawasaki, D., Miura, N., Sato, T. et Ito, A. Mécanismes d'action anti-arthritiques du sulfate de chondroïtine naturel dans les chondrocytes articulaires humains et les fibroblastes synoviaux. Biol.Pharm Bull. 2010;33:410-414. Voir résumé.
- Pavelka, K., Coste, P., Geher, P. et Krejci, G. Efficacité et innocuité de la piasclédine 300 versus sulfate de chondroïtine dans un traitement de 6 mois plus 2 mois d'observation chez des patients souffrant d'arthrose du genou. Clin.Rhumatol. 2010;29:659-670. Voir résumé.
- Tat, S. K., Pelletier, J. P., Mineau, F., Duval, N. et Martel-Pelletier, J. Effets variables de 3 composés de sulfate de chondroïtine différents sur le cartilage/chondrocytes arthrosiques humains : pertinence de la pureté et du processus de production. J.Rhumatol. 2010;37:656-664. Voir résumé.
- Lane, S. S., Naylor, D. W., Kullerstrand, L. J., Knauth, K. et Lindstrom, R. L. Comparaison prospective des effets d'Occucoat, Viscoat et Healon sur la pression intraoculaire et la perte de cellules endothéliales. J Cataract Refract.Surg. 1991;17:21-26. Voir résumé.
- Jackson, CG, Plaas, AH, Sandy, JD, Hua, C., Kim-Rolands, S., Barnhill, JG, Harris, CL et Clegg, DO La pharmacocinétique humaine de l'ingestion orale de glucosamine et de sulfate de chondroïtine pris séparément ou en combinaison. Arthrose Cartilage 2010;18:297-302. Voir résumé.
- Black, C., Clar, C., Henderson, R., MacEachern, C., McNamee, P., Quayyum, Z., Royle, P. et Thomas, S. L'efficacité clinique des suppléments de glucosamine et de chondroïtine pour ralentir ou arrêter la progression de l'arthrose du genou : une revue systématique et une évaluation économique. Évalu.Technologie de la santé. 2009;13:1-148. Voir résumé.
- Sasisekharan, R. et Shriver, Z. De la crise à l'opportunité : une perspective sur la crise de l'héparine. Thromb.Haemost. 2009;102:854-858. Voir résumé.
- Crowley, DC, Lau, FC, Sharma, P., Evans, M., Guthrie, N., Bagchi, M., Bagchi, D., Dey, DK et Raychaudhuri, SP Sécurité et efficacité du collagène de type II non dénaturé dans le traitement de l'arthrose du genou : un essai clinique. Int.J.Med.Sci. 2009;6:312-321. Voir résumé.
- Rainsford, K. D. Importance de la composition pharmaceutique et des preuves issues d'essais cliniques et d'études pharmacologiques pour déterminer l'efficacité du sulfate de chondroïtine et d'autres glycosaminoglycanes : une critique. J.Pharm.Pharmacol. 2009;61:1263-1270. Voir résumé.
- Hauser, P. J., Buethe, D. A., Califano, J., Sofinowski, T. M., Culkin, D. J. et Hurst, R. E. Restauration de la fonction de barrière à la vessie endommagée par l'acide par le sulfate de chondroïtine intravésical. J.Urol. 2009;182:2477-2482. Voir résumé.
- Kubo, M., Ando, K., Mimura, T., Matsusue, Y. et Mori, K. Sulfate de chondroïtine pour le traitement de l'arthrose de la hanche et du genou : état actuel et tendances futures. Science de la vie. 9-23-2009;85(13-14):477-483. Voir résumé.
- Lee, Y. H., Woo, J. H., Choi, S. J., Ji, J. D. et Song, G. G. Effet de la glucosamine ou du sulfate de chondroïtine sur la progression de l'arthrose : une méta-analyse. Rheumatol Int 2010;30:357-363. Voir résumé.
- du Souich, P., Garcia, A. G., Verges, J. et Montell, E. Effets immunomodulateurs et anti-inflammatoires du sulfate de chondroïtine. J.Cell Mol.Med. 2009;13(8A):1451-1463. Voir résumé.
- Fthenou, E., Zong, F., Zafiropoulos, A., Dobra, K., Hjerpe, A. et Tzanakakis, G. N. Le sulfate de chondroïtine A régule l'adhésion, la motilité et la migration cellulaires du fibrosarcome via les voies de signalisation JNK et tyrosine kinase. In Vivo 2009;23:69-76. Voir résumé.
- Bhattacharyya, S., Solakyildirim, K., Zhang, Z., Chen, ML, Linhardt, RJ et Tobacman, JK Augmentation de l'IL-8 liée aux cellules dans les cellules épithéliales bronchiques après l'extinction de l'arylsulfatase B en raison de la séquestration avec la chondroïtine-4- sulfate. Am.J.Respir.Cell Mol.Biol. 2010;42:51-61. Voir résumé.
- Schulz, A., Vestweber, A. M. et Dressler, D. [Action anti-inflammatoire d'une préparation de sulfate d'acide hyaluronique et de chondroïtine dans un modèle de vessie in vitro]. Aktuelle Urol. 2009;40:109-112. Voir résumé.
- David-Raoudi, M., Deschrevel, B., Leclercq, S., Galera, P., Boumediene, K., and Pujol, JP Le sulfate de chondroïtine augmente la production d'hyaluronane par les synoviocytes humains via une régulation différentielle des hyaluronanes synthases : rôle de p38 et Akt. Arthrite Rheum. 2009;60:760-770. Voir résumé.
- Matsuno, H., Nakamura, H., Katayama, K., Hayashi, S., Kano, S., Yudoh, K. et Kiso, Y. Effets d'une administration orale de glucosamine-chondroïtine-quercétine glucoside sur la synoviale propriétés fluides chez les patients souffrant d'arthrose et de polyarthrite rhumatoïde. Biosci.Biotechnol.Biochem. 2009;73:288-292. Voir résumé.
- Kahan, A., Uebelhart, D., De, Vathaire F., Delmas, P.D., et Reginster, J. Y. Effets à long terme du sulfate de chondroïtine 4 et 6 sur l'arthrose du genou: l'étude sur la prévention de la progression de l'arthrose, un essai randomisé, en double aveugle, contrôlé par placebo sur deux ans. Arthrite Rheum. 2009;60:524-533. Voir résumé.
- Rovetta, G. Galactosaminoglycuronoglycan sulfate (matrice) dans le traitement de l'arthrose tibio-fibulaire du genou. Drugs Exp Clin Res 1991;17:53-57. Voir résumé.
- Oliviero, U., Sorrentino, GP, De Paola, P., Tranfaglia, E., D'Alessandro, A., Carifi, S., Porfido, FA, Cerio, R., Grasso, AM, Policicchio, D., et . Effets du traitement avec matrice sur les personnes âgées atteintes de dégénérescence articulaire chronique. Drugs Exp Clin Res 1991;17:45-51. Voir résumé.
- Bruyere, O., Burlet, N., Delmas, P. D., Rizzoli, R., Cooper, C. et Reginster, J. Y. Évaluation des médicaments symptomatiques à action lente dans l'arthrose à l'aide du système GRADE. BMC.Musculosquelette.Disord. 2008;9:165. Voir résumé.
- Theoharides, T. C., Kempuraj, D., Vakali, S. et Sant, G. R. Traitement de la cystite interstitielle réfractaire/syndrome de la vessie douloureuse avec CystoProtek - un supplément naturel multi-agents oral. Can J Urol 2008;15:4410-4414. Voir résumé.
- Hochberg, M. C., Zhan, M. et Langenberg, P. Le taux de diminution de la largeur de l'espace articulaire chez les patients souffrant d'arthrose du genou : une revue systématique et une méta-analyse d'essais randomisés contrôlés par placebo sur le sulfate de chondroïtine. Curr.Med.Res.Opin. 2008;24:3029-3035. Voir résumé.
- Sawitzke, AD, Shi, H., Finco, MF, Dunlop, DD, Bingham, CO, III, Harris, CL, Singer, NG, Bradley, JD, Silver, D., Jackson, CG, Lane, NE, Oddis, CV, Wolfe, F., Lisse, J., Furst, DE, Reda, DJ, Moskowitz, RW, Williams, HJ et Clegg, DO L'effet de la glucosamine et/ou du sulfate de chondroïtine sur la progression de l'arthrose du genou : un rapport de l'essai d'intervention sur l'arthrite glucosamine/chondroïtine. Arthrite Rheum. 2008;58:3183-3191. Voir résumé.
- Nickel, JC, Egerdie, B., Downey, J., Singh, R., Skehan, A., Carr, L. et Irvine-Bird, K. Une étude de pratique clinique multicentrique en vie réelle pour évaluer l'efficacité et l'innocuité de sulfate de chondroïtine intravésicale pour le traitement de la cystite interstitielle. BJU.Int. 2009;103:56-60. Voir résumé.
- Nordling, J. et van, Ophoven A. Reconstitution intravésicale de glycosaminoglycanes avec du sulfate de chondroïtine dans les formes chroniques de cystite. Un essai clinique observationnel prospectif, multinational et multicentrique. Arzneimittelforschung. 2008;58:328-335. Voir résumé.
- Theocharis, D.A., Skandalis, S.S., Noulas, A.V., Papageorgakopoulou, N., Theocharis, A.D. et Karamanos, N.K. Hyaluronan et chondroïtine sulfate protéoglycanes dans l'organisation supramoléculaire du corps vitré des mammifères. Connect.Tissu Res. 2008;49:124-128. Voir résumé.
- Fosang, A. J. et Little, C. B. Aperçu des médicaments : les aggrécanases en tant que cibles thérapeutiques pour l'arthrose. Nat.Clin.Pratique.Rheumatol. 2008;4:420-427. Voir résumé.
- Praveen, M. R., Koul, A., Vasavada, A. R., Pandita, D., Dixit, N. V. et Dahodwala, F. F. DisCoVisc versus la technique soft-shell utilisant Viscoat et Provisc dans la phacoémulsification : essai clinique randomisé. J. Cataract Refract.Surg. 2008;34:1145-1151. Voir résumé.
- Dudics, V., Kunstar, A., Kovacs, J., Lakatos, T., Geher, P., Gomor, B., Monostori, E. et Uher, F. Potentiel chondrogène des cellules souches mésenchymateuses de patients atteints de rhumatisme Arthrite et arthrose : mesures dans un système de microculture. Cellules Tissus.Organes 2009;189:307-316. Voir résumé.
- Porru, D., Cervigni, M., Nasta, L., Natale, F., Lo, Voi R., Tinelli, C., Gardella, B., Anghileri, A., Spinillo, A., et Rovereto, B. Résultats de l'acide hyaluronique endovésical/sulfate de chondroïtine dans le traitement de la cystite interstitielle/syndrome de la vessie douloureuse. Rev.Recent Clin.Trials 2008;3:126-129. Voir résumé.
- Cervigni, M., Natale, F., Nasta, L., Padoa, A., Voi, R. L. et Porru, D. Une thérapie intravésicale combinée avec de l'acide hyaluronique et de la chondroïtine pour le syndrome douloureux réfractaire de la vessie/cystite interstitielle. Int.Urogynecol.J.Pelvic.Floor.Dysfunct. 2008;19:943-947. Voir résumé.
- Zhang, W., Moskowitz, RW, Nuki, G., Abramson, S., Altman, RD, Arden, N., Bierma-Zeinstra, S., Brandt, KD, Croft, P., Doherty, M., Dougados , M., Hochberg, M., Hunter, DJ, Kwoh, K., Lohmander, LS et Tugwell, P. Recommandations de l'OARSI pour la prise en charge de l'arthrose de la hanche et du genou, Partie II : Lignes directrices de consensus d'experts fondées sur des preuves de l'OARSI. Arthrose.Cartilage. 2008;16:137-162. Voir résumé.
- Rainer, G., Stifter, E., Luksch, A. et Menapace, R. Comparaison de l'effet de Viscoat et DuoVisc sur la pression intraoculaire postopératoire après une chirurgie de la cataracte par petite incision. J. Cataract Refract.Surg. 2008;34:253-257. Voir résumé.
- Laroche, L., Arrata, M., Brasseur, G., Lagoutte, F., Le Mer, Y., Lumbroso, P., Mercante, M., Normand, F., Rigal, D., Roncin, S. , et . Traitement du syndrome de l'œil sec par gel lacrymal : étude multicentrique randomisée. J Fr.Ophtalmol. 1991;14:321-326. Voir résumé.
- Conte, A., de Bernardi, M., Palmieri, L., Lualdi, P., Mautone, G. et Ronca, G. Le destin métabolique du sulfate de chondroïtine exogène chez l'homme. Arzneimittelforschung. 1991;41:768-772. Voir résumé.
- Bana, G., Jamard, B., Verrouil, E., et Mazières, B. Sulfate de chondroïtine dans la prise en charge de l'arthrose de la hanche et du genou : un aperçu. Adv.Pharmacol. 2006;53:507-522. Voir résumé.
- Mazieres, B., Hucher, M., Zaim, M. et Garnero, P. Effet du sulfate de chondroïtine dans l'arthrose symptomatique du genou : une étude multicentrique, randomisée, en double aveugle, contrôlée par placebo. Ann Rheum Dis 2007;66:639-645. Voir résumé.
- Braun, W. A., Flynn, M. G., Armstrong, W. J. et Jacks, D. D. Les effets de la supplémentation en sulfate de chondroïtine sur les indices de dommages musculaires induits par l'exercice excentrique des bras. J.Sports Med.Phys.Fitness 2005;45:553-560. Voir résumé.
- Michel, BA, Stucki, G., Frey, D., De, Vathaire F., Vignon, E., Bruehlmann, P., et Uebelhart, D. Chondroïtines 4 et 6 sulfate dans l'arthrose du genou : une étude randomisée, contrôlée essai. Arthrite Rheum. 2005;52:779-786. Voir résumé.
- Rovetta, G., Monteforte, P., Molfetta, G. et Balestra, V. Une étude de deux ans sur le sulfate de chondroïtine dans l'arthrose érosive des mains : comportement des érosions, des ostéophytes, de la douleur et du dysfonctionnement de la main. Drugs Exp Clin Res 2004;30:11-16. Voir résumé.
- Mathieu, P. Progression radiologique de l'arthrose fémoro-tibiale interne dans la gonarthrose. Effet chondro-protecteur des sulfates de chondroïtine ACS4-ACS6]. Presse Med 9-14-2002;31:1386-1390. Voir résumé.
- Volpi, N. Biodisponibilité orale du sulfate de chondroïtine (Condrosulf) et de ses constituants chez des volontaires masculins en bonne santé. Arthrose.Cartilage. 2002;10:768-777. Voir résumé.
- Rovetta, G., Monteforte, P., Molfetta, G. et Balestra, V. Chondroïtine sulfate dans l'arthrose érosive des mains. Int J Tissue React. 2002;24:29-32. Voir résumé.
- Steinhoff, G., Ittah, B. et Rowan, S. L'efficacité du sulfate de chondroïtine à 0,2% dans le traitement de la cystite interstitielle. Can J Urol 2002;9:1454-1458. Voir résumé.
- O'Rourke, M. Détermination de l'efficacité de la glucosamine et de la chondroïtine pour l'arthrose. Nurse Pract 2001;26:44-52. Voir résumé.
- [Effets bénéfiques de Chondrosulf 400 sur la douleur et la fonction articulaire dans l'arthrose : une méta-analyse]. Presse Med 2000;29(27 Suppl):19-20. Voir résumé.
- Etude multicentrique européenne sur l'efficacité du sulfate de chondroïtine dans la gonarthrose : un nouveau regard sur les résultats biochimiques et radiologiques. Presse Med 2000;29(27 Suppl):15-18. Voir résumé.
- Alekseeva, L. I., Benevolenskaia, L. I., Nasonov, E. L., Chichasova, N. V. et Kariakin, A. N. [Structum (chondroïtine sulfate) - un nouvel agent pour le traitement de l'arthrose]. Ter.Arkh. 1999;71:51-53. Voir résumé.
- Schwartz SR, Park J. Ingestion de BioCell Collagen, un nouvel extrait de cartilage sternal de poulet hydrolysé ; microcirculation sanguine améliorée et signes de vieillissement du visage réduits. Clin Interv Vieillissement. 2012;7:267-273. Voir résumé.
- Schauss AG, Stenehjem J, Park J, Endres JR, Clewell A. Effet du nouvel extrait de cartilage sternal de poulet hydrolysé de faible poids moléculaire, BioCell Collagen, sur l'amélioration des symptômes liés à l'arthrose : un essai randomisé, en double aveugle, contrôlé par placebo. J Agric Food Chem. 2012;60:4096-4101. Voir résumé.
- Kalman DS, Schwartz HI, Pachon J, Sheldon E, Almada AL. Un essai clinique pilote randomisé en double aveugle évaluant l'innocuité et l'efficacité du collagène hydrolysé de type II chez les adultes souffrant d'arthrose. FASEB Experimental Biology 2004, résumés, Washington DC, 17-21 avril 2004; A90.
- Verges J, Montell E, Herrero M, et al. Améliorations cliniques et histopathologiques du psoriasis avec le sulfate de chondroïtine par voie orale : une découverte fortuite. Dermatol en ligne J 2005;11:31. Voir résumé.
- Burke S, Sugar J, Farber MD. Comparaison des effets de deux agents viscoélastiques, Healon et Viscoat sur la pression intraoculaire postopératoire après kératoplastie pénétrante. Ophthalmic Surg 1990;21:821-6. Voir résumé.
- Zhang YX, Dong W, Liu H et al. Effets du sulfate de chondroïtine et de la glucosamine chez les patients adultes atteints de la maladie de Kashin-Beck. Clin Rheumatol 2010;29:357-62. Voir résumé.
- Gauruder-Burmester A, Popken G. Suivi à 24 mois après traitement de la vessie hyperactive avec 0,2% de sulfate de chondroïtine de sodium. Aktuelle Urol 2009;40:355-9. Voir résumé.
- Uebelhart D, Knussel O, Theiler R. Efficacité et tolérance d'un sulfate de chondroïtine aviaire par voie orale dans l'arthrose douloureuse du genou [résumé]. Schweiz Med Wochenschr 1999;129:1174.
- Leeb BF, Petera P, Neumann K. Résultats d'une étude multicentrique sur l'utilisation du sulfate de chondroïtine (Condrosulf) dans l'arthrose des articulations des doigts, du genou et de la hanche. Wien Med Wochenschr 1996;146:609-14. Voir résumé.
- Gabay C, Medinger-Sadowski C, Gascon D, et al. Effet symptomatique de la chondroïtine 4 et du sulfate de chondroïtine 6 sur l'arthrose de la main : un essai clinique randomisé, en double aveugle, contrôlé par placebo dans un seul centre. Arthritis Rheum 2011;63:3383-91. Voir résumé.
- Yue QY, Strandell J, Myrberg O. L'utilisation concomitante de glucosamine peut potentiellement provoquer l'effet de la warfarine. L'Observatoire d'Uppsala. Disponible sur : www.who-umc.org/graphics/9722.pdf (consulté le 28 avril 2008).
- Knudsen J, Sokol GH. Interaction potentielle glucosamine-warfarine entraînant une augmentation du rapport international normalisé : rapport de cas et revue de la littérature et de la base de données MedWatch. Pharmacothérapie 2008;28:540-8. Voir résumé.
- Reichenbach S, Sterchi R, Scherer M, et al. Méta-analyse : chondroïtine pour l'arthrose du genou ou de la hanche. Ann Intern Med 2007;146:580-90. Voir résumé.
- Messier SP, Mihalko S, Loeser RF et al. Glucosamine/chondroïtine associée à l'exercice pour le traitement de l'arthrose du genou : une étude préliminaire. Arthrose Cartilage 2007;15:1256-66. Voir résumé.
- Kahan A. STOPP (ETUDE sur la prévention de la progression de l'arthrose) : un nouvel essai de deux ans avec le sulfate de chondroïtine 4&6 (CS). Disponible sur : www.ibsa-ch.com/eular_2006_amsterdam_vignon-2.pdf (consulté le 25 avril 2007).
- Huang J, Olivenstein R, Taha R, et al. Dépôt accru de protéoglycanes dans la paroi des voies respiratoires des asthmatiques atopiques. Am J Respir Crit Care Med 1999;160:725-9. Voir résumé.
- Clegg DO, Reda DJ, Harris CL, et al. Glucosamine, sulfate de chondroïtine et les deux en association pour l'arthrose douloureuse du genou. N Engl J Med 2006;354:795-808. Voir résumé.
- Uebelhart D, Malaise M, Marcolongo R, et al. Traitement intermittent de l'arthrose du genou avec du sulfate de chondroïtine par voie orale : étude multicentrique, randomisée, en double aveugle versus placebo d'un an. Arthrose Cartilage 2004;12:269-76. Voir résumé.
- Sakko AJ, Ricciardelli C, Mayne K, et al. Modulation de l'attachement des cellules cancéreuses de la prostate à la matrice par versican. Cancer Res 2003;63:4786-91. Voir résumé.
- Rozenfeld V, Crain JL, Callahan AK. Augmentation possible de l'effet de la warfarine par la glucosamine-chondroïtine. Am J Health Syst Pharm 2004;61:306-307. Voir résumé.
- Di Caro A, Perola E, Bartolini B, et al. Des fractions de sulfates de galactosaminoglycane chimiquement sursulfatés inhibent trois virus enveloppés : le virus de l'immunodéficience humaine de type 1, le virus de l'herpès simplex de type 1 et le cytomégalovirus humain. Antivir Chem Chemother 1999;10:33-8.. Voir le résumé.
- Danao-Camara T. Effets secondaires potentiels du traitement à la glucosamine et à la chondroïtine. Arthrite Rheum 2000;43:2853. Voir résumé.
- Cohen M, Wolfe R, Mai T, Lewis D. Un essai randomisé, en double aveugle, contrôlé par placebo d'une crème topique contenant du sulfate de glucosamine, du sulfate de chondroïtine et du camphre pour l'arthrose du genou. J Rheumatol 2003;30:523-8.. Voir le résumé.
- Baici A, Horler D, Moser B, et al. Analyse des glycosaminoglycanes dans le sérum humain après administration orale de sulfate de chondroïtine. Rheumatol Int 1992;12:81-8.. Voir le résumé.
- Richy F, Bruyère O, Ethgen O, et al. Efficacité structurelle et symptomatique de la glucosamine et de la chondroïtine dans l'arthrose du genou : une méta-analyse complète. Arch Intern Med 2003;163:1514-22. Voir résumé.
- Henry-Launois B. Evaluation de l'utilisation de l'impact financier du Chondrosulf 400 dans la pratique médicale actuelle. Une partie des Actes d'un Symposium Scientifique tenu au XIth EULAR Symposium : Nouvelles approches dans l'arthrose : Chondroïtine sulfate (CS 4&6) pas seulement un traitement symptomatique. Genève, 1998.
- Verbruggen G, Goemaere S, Veys EM. Systèmes pour évaluer la progression de l'arthrose des articulations des doigts et les effets des médicaments modificateurs de la maladie contre l'arthrose. Clin Rheumatol 2002;21:231-43. Voir résumé.
- Tallia AF, Cardone DA. Exacerbation de l'asthme associée à un supplément de glucosamine-chondroïtine. J Am Board Fam Pract 2002;15:481-4.. Voir le résumé.
- Ricciardelli C, Quinn DI, Raymond WA, et al. Des niveaux élevés de sulfate de chondroïtine péritumoral sont prédictifs d'un mauvais pronostic chez les patients traités par prostatectomie radicale pour un cancer de la prostate à un stade précoce. Cancer Res 1999;59:2324-8. Voir résumé.
- Ylisastigui L, Bakri Y, Amzazi S, et al. Glycosaminoglycanes solubles Ne potentialisent pas l'activité antivirale de RANTES sur l'infection des macrophages primaires par le virus de l'immunodéficience humaine de type 1. Virologie 2000;278:412-22. Voir résumé.
- Adebowale AO, Cox DS, Liang Z, et al. Analyse de la teneur en glucosamine et en sulfate de chondroïtine des produits commercialisés et de la perméabilité Caco-2 des matières premières en sulfate de chondroïtine. JANA 2000;3:37-44.
- Cao LC, Boeve ER, de Bruijn WC, et al. Glycosaminoglycanes et polysaccharides sulfatés semi-synthétiques : aperçu de leur application potentielle dans le traitement des patients atteints de lithiase urinaire. Urologie 1997;50:173-83. Voir résumé.
- Morrison LM. Traitement de la maladie coronarienne artérioscléreuse avec du sulfate de chondroïtine-A : rapport préliminaire. J Am Geriatr Soc 1968;16:779-85. Voir résumé.
- Morrison LM, Bajwa GS, Alfin-Slater RB, Ershoff BH. Prévention des lésions vasculaires par la chondroïtine sulfate A dans l'artère coronaire et l'aorte de rats induites par une hypervitaminose D, régime riche en cholestérol. Athérosclérose 1972;16:105-18. Voir résumé.
- Mazières B, Combe B, Phan Van A, et al. Sulfate de chondroïtine dans l'arthrose du genou : une étude clinique multicentrique prospective, en double aveugle, contrôlée par placebo. J Rheumatol 2001;28:173-81. Voir résumé.
- Das A Jr, Hammad TA. Efficacité d'une combinaison de chlorhydrate de glucosamine FCHG49, de sulfate de chondroïtine sodique de bas poids moléculaire TRH122 et d'ascorbate de manganèse dans la gestion de l'arthrose du genou. Arthrose Cartilage 2000;8:343-50. Voir résumé.
- Conseil de l'alimentation et de la nutrition, Institut de médecine. Apports nutritionnels de référence pour la vitamine A, la vitamine K, l'arsenic, le bore, le chrome, le cuivre, l'iode, le fer, le manganèse, le molybdène, le nickel, le silicium, le vanadium et le zinc. Washington, DC : National Academy Press, 2002. Disponible sur : www.nap.edu/books/0309072794/html/.
- Pipitone VR. Chondroprotection avec du sulfate de chondroïtine. Drugs Exp Clin Res 1991;17:3-7. Voir résumé.
- Leffler CT, Philippi AF, Leffler SG, et al. Ascorbate de glucosamine, de chondroïtine et de manganèse pour la maladie dégénérative des articulations du genou ou du bas du dos : une étude pilote randomisée, en double aveugle et contrôlée par placebo. Mil Med 1999;164:85-91. Voir résumé.
- Silvestro L, Lanzarotti E, Marchi E, et al. Pharmacocinétique humaine des glycosaminoglycanes utilisant des substances marquées et non marquées au deutérium : preuves d'absorption orale. Semin Thromb Hemost 1994;20:281-92. Voir résumé.
- Conte A, Volpi N, Palmieri L, et al. Aspects biochimiques et pharmacocinétiques du traitement oral avec du sulfate de chondroïtine. Arzneimittelforschung 1995;45:918-25. Voir résumé.
- Ronca F, Palmieri L, Panicucci P, et al. Activité anti-inflammatoire du sulfate de chondroïtine. Arthrose Cartilage 1998;6 Suppl A:14-21. Voir résumé.
- Andermann G, Dietz M. L'influence de la voie d'administration sur la biodisponibilité d'une macromolécule endogène : la chondroïtine sulfate (CSA). Eur J Drug Metab Pharmacokinet 1982;7:11-6. Voir résumé.
- Conte A, de Bernardi M, Palmieri L, et al. Devenir métabolique du sulfate de chondroïtine exogène chez l'homme. Arzneimittelforschung 1991; 41:768-72. Voir résumé.
- McAlindon TE, député de LaValley, Gulin JP, Felson DT. Glucosamine et chondroïtine pour le traitement de l'arthrose : une évaluation systématique de la qualité et une méta-analyse. JAMA 2000;283:1469-75. Voir résumé.
- Limberg MB, McCaa C, Kissling GE, Kaufman HE. Application topique d'acide hyaluronique et de sulfate de chondroïtine dans le traitement de la sécheresse oculaire. Am J Ophthalmol 1987;103:194-7. Voir résumé.
- Kelly GS. Le rôle du sulfate de glucosamine et des sulfates de chondroïtine dans le traitement des maladies dégénératives des articulations. Altern Med Rev 1998;3:27-39. Voir résumé.
- Bucsi L, Poor G. Efficacité et tolérance du sulfate de chondroïtine par voie orale en tant que médicament symptomatique à action lente pour l'arthrose (SYSADOA) dans le traitement de l'arthrose du genou. Arthrose Cartilage 1998;6 Suppl A:31-6. Voir résumé.
- Bourgeois P, Chales G, Dehais J, et al. Efficacité et tolérance du sulfate de chondroïtine 1200 mg/jour vs sulfate de chondroïtine 3 x 400 mg/jour vs placebo. Arthrose Cartilage 1998;6:25-30. Voir résumé.
- Uebelhart D, Thonar EJ, Delmas PD, et al. Effets du sulfate de chondroïtine par voie orale sur la progression de l'arthrose du genou : une étude pilote. Arthrose Cartilage 1998;6:39-46. Voir résumé.
- Morrison LM, Enrick N. Maladie coronarienne: réduction du taux de mortalité par le sulfate de chondroïtine A. Angiology 1973;24:269-87. Voir résumé.
- Le juge en chef Lewis. Lettre pour réitérer certaines préoccupations de santé publique et de sécurité aux entreprises fabriquant ou important des compléments alimentaires contenant des tissus bovins spécifiques.FDA. Disponible sur : www.cfsan.fda.gov/~dms/dspltr05.html.
- Leeb BF, Schweitzer H, Montag K, Smolen JS. Une méta-analyse du sulfate de chondroïtine dans le traitement de l'arthrose. J Rheumatol 2000;27:205-11. Voir résumé.
- Bagasra O, Whittle P, Heins B, Pomerantz RJ. Activité anti-virus de l'immunodéficience humaine de type 1 des monosaccharides sulfatés : comparaison avec les polysaccharides sulfatés et autres polyions. J Infect Dis 1991;164:1082-90. Voir résumé.
- Jurkiewicz E, Panse P, Jentsch KD, et al. Activité anti-VIH-1 in vitro du polysulfate de chondroïtine. SIDA 1989;3:423-7. Voir résumé.
- Chavez ML. Sulfate de glucosamine et sulfates de chondroïtine. Hosp Pharm 1997;32:1275-85.
- Mazières B, Loyau G, Menkes CJ, et al. Le sulfate de chondroïtine dans le traitement de la gonarthrose et de la coxarthrose. résultat à 5 mois d'une étude prospective multicentrique contrôlée en double aveugle utilisant un placebo]. Rev Rhum Mal Osteoartic 1992;59:466-72. Voir résumé.
- Conrozier T. [Traitements anti-arthrosiques : efficacité et tolérance des sulfates de chondroïtine]. Presse Med 1998;27:1862-5. Voir résumé.
- Morreale P, Manopulo R, Galati M, et al. Comparaison de l'efficacité anti-inflammatoire du sulfate de chondroïtine et du diclofénac sodique chez les patients atteints d'arthrose du genou. J Rheumatol 1996;23:1385-91. Voir résumé.